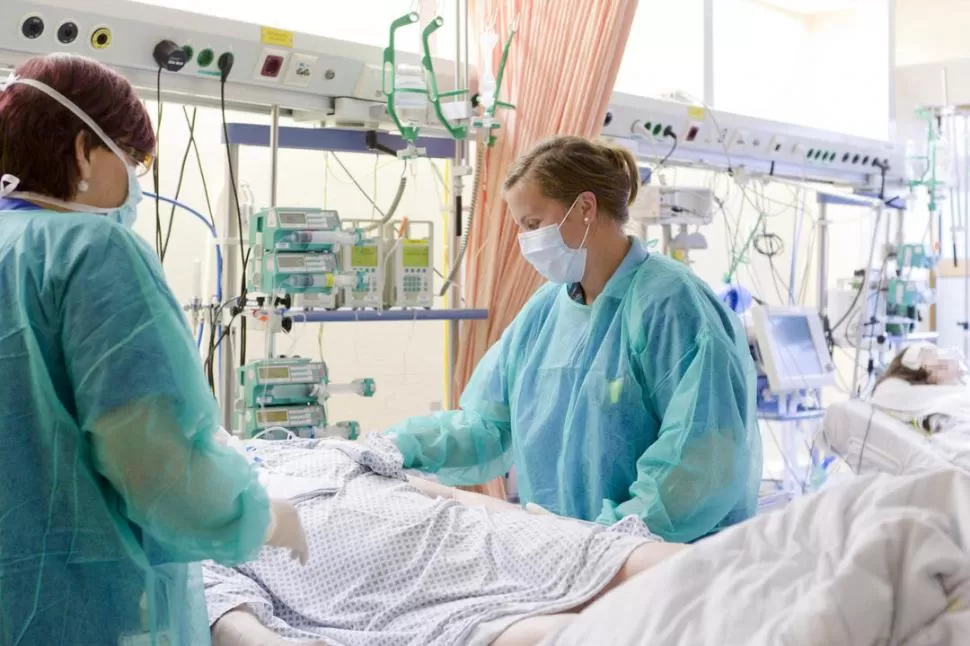
 EN RIESGO. Las prácticas de terapia intensiva necesitan estar libres de gérmenes para poder ser llevadas a cabo.
EN RIESGO. Las prácticas de terapia intensiva necesitan estar libres de gérmenes para poder ser llevadas a cabo.
Las bacterias son fundamentales para nuestra vida, siempre y cuando se mantengan en equilibrio. Pero cuando este se rompe generan enfermedades, muchas de las cuales, durante milenios, fueron mortales.
En septiembre de 1928 Alexander Fleming descubrió la penicilina, y marcó un quiebre en la historia de la medicina y de la salud pública: abría la posibilidad de combatir infecciones como neumonías y hasta heridas infectadas, que hasta entonces podían costar la vida.
Menos de un siglo después, los antibióticos se están volviendo impotentes: las bacterias son cada vez más resistentes a ellos, e incluso algunas se han vuelto invencibles. Este problema, conocido como resistencia antimicrobiana, es hoy responsable de unas 700.000 muertes anuales, y se calcula que en 2050 la cifra llegará a 10 millones. La Organización Mundial de la Salud (OMS) lleva años alertando sobre la gravedad del problema.
Así las cosas, resulta indispensable hallar pronto una salida. De lo contrario, la medicina -tal como la conocemos- dejará de funcionar.
“Muchas prácticas, como la diálisis y la quimioterapia, que deben estar libres de gérmenes, no se podrán hacer”, advirtió Alejandra Corso, jefa del Servicio de Antimicrobianos de la Administración Nacional de Laboratorios e Institutos de Salud del Malbrán, según la agencia de noticias de la Universidad de San Martín.
Por suerte, al menos por ahora, las noticias malas y las buenas más o menos se alternan.
El 11 de julio había caído como una bomba la noticia de que Novartis, líder suizo del sector farmacia, había clausurado su línea de investigación y desarrollo de nuevos antibacterianos (es el cuarto laboratorio que renuncia a intentarlo).
En contraposición, hace unos días Pfizer lanzó en Buenos Aires un medicamento que Francisco Nacinovich, jefe de Infectología del Instituto Cardiovascular de Buenos Aires, llamó “bala de plata” (por tradición, la única “capaz de matar” hombres-lobo y brujas).
El medicamento (que combina un antibiótico y un inhibidor de enzimas) puede combatir la gran “bruja” de los hospitales de todo el mundo: una bacteria que tiene un nombre difícil (Klebsiella pneumoniae resistente a Carbapenems), así que para nombrarla se inventó un acrónimo (KPC) y por suerte, ahora, también un tratamiento.
“El mecanismo de resistencia es un modo normal de supervivencia de las bacterias. Pero el uso indebido e indiscriminado de antibióticos ha fortalecido esa capacidad de mutar para defenderse”, explicó durante la presentación, de la que participó LA GACETA, Fernando Pasteran, especialista en Microbiología Clínica del Servicio de Antimicrobianos del Laboratorio Nacional de Referencia del Instituto Nacional de Enfermedades Infecciosas, también del Malbrán.
“Necesitamos nuevos antibióticos para luchar contra las infecciones hospitalarias causadas por gérmenes resistentes. Hasta ahora no disponíamos de suficientes alternativas terapéuticas efectivas y tolerables para el paciente”, añadió.
En el nuevo medicamento, cada una de las moléculas cumple su tarea. “Usamos un antibiótico (ceftazidima) que solo ya no funciona en caso de bacterias multirresistentes: su mecanismo de acción ha sido detectado por ellas, y se defienden produciendo enzimas (moléculas de proteína) que contrarrestan su efecto -explicó Carolina Pein, directora médica de la línea hospitalaria del laboratorio durante la presentación-. Lo que se hizo fue combinarlo con el avibactam, que es un inhibidor de la enzima. Y así el antibiótico recupera su eficacia”.
El chicle que distrae
“Las dos drogas van juntas; de hecho, forman una nueva familia química. El avibactam ‘alimenta’ la bacteria con algo diferente de la proteína y ‘la engaña’... Como si le diéramos chicle para masticar cuando tiene hambre”, explicó muy pedagógicamente Pasteran. “Y la bacteria, distraída, no se dedica a resistirse al antibiótico -añadió, y bromeó: En confianza, les decimos ‘caz’ y ‘avi’”.
La realidad argentina
“Estamos muy entusiasmados con esta nueva alternativa terapéutica -resaltó Nacinovich-. Es una herramienta segura y efectiva contra gérmenes muy difíciles de tratar, y que representan un serio y creciente problema de salud en nuestro país”.
De hecho, en la Argentina KPC es uno de los patógenos que genera mayor preocupación, pues ha sido detectado en las 24 provincias (la primera notificación de su presencia es de 2006), y representa más del el 30% de los casos de Klebsiella pneumoniae confirmados. Causa el 50% de las infecciones severas, provoca infecciones asociadas con altas tasas de morbilidad y mortalidad, y es resistente a casi todos los antibióticos disponibles, destacó Pasteran.
“Su mecanismo de resistencia se conoció en 2001, y desde entonces se dispersó por todo el planeta. Y no sólo la bacteria: ella contagia a otras ese mecanismo -alertó-. Y nadie está a salvo: la resistencia a los antibióticos es muy grave y no discrimina”.















